PROCESSUS et CONSEQUENCES de la POLLUTION ORGANIQUE.*
S’il n’y a pas d’apport de produits azotés en excès dans un milieu aquatique, le cycle de l’azote dans le « système » est équilibré, il ne se produit aucun désordre, on ne constate aucune pollution. Dans la rivière la matière organique peut être naturellement décomposée en raison de la présence d’oxygène dissous et transformée dans le processus du CYCLE DE L’AZOTE pour être finalement assimilée par les plantes aquatiques lors de leur croissance après transformation en nitrates.
A l’inverse, l’excès d’apports organiques entraînera des conséquences à chaque étape du cycle de l’azote :
AU STADE DE LA MATIÈRE ORGANIQUE
Les rejets résiduaires des égouts des agglomérations, surtout s’il n’y a pas de station d’épuration, apportent de très grandes quantités de matières organiques (M.O.) aux rivières (excréments, eaux sanitaires, de cuisine, de salle de bains, eaux usées d’activités alimentaires,….) Cette surabondance perturbe le cycle de l’azote et le fonctionnement de la rivière.
La pollution organique peur provenir également des rejets agricoles (lisier, purin), industriels de type alimentaire ( conserverie, laiteries, fromageries, atelier vinicoles, …) ou de transformations de produits végétaux (papeterie, …) La présence de traces de boues organiques visibles dans le lit d’une rivière est inacceptable et dénonce bien souvent la proximité d’un rejet d’égouts non épuré

Une présence trop importance de M.O. en suspension dans la rivière milieu contribue à en appauvrir les eaux en oxygène dissous(O2). Cet oxygène est indispensable à la vie des animaux aquatiques mais également à celle des bactéries aérobies (qui respirent de l’oxygène) qui transforment la matière organique en ammonium, nitrites, nitrates. Ainsi l’excès de M.O. restreint le processus d’auto-épuration.
(voir: oxygène dissous dans la page concernées aux PARAMETRES
Lorsque des amoncellements de boues riches en matières organiques se constituent au fond d’un cours d’eau, ces M.O. peuvent être décomposées par les bactéries en anaérobiose (c’est à dire sans air) en produisant des dégagement gazeux putrides : méthane, gaz carbonique et hydrogène sulfuré nocif pour la vie aquatique.
Pour estimer l’importance des MO présentes en solution dans l’eau , on utilise deux méthodes de mesure indirectes. Elles consistent à déterminer la quantité d’oxygène nécessaire à leur décomposition :
– La mesure de la DCO ( Demande Biochimique en Oxygène) permet de mesurer la quantité d’oxygène nécessaire à l’oxydation à chaud sous l’action d’un oxydant chimique de la totalité des substances oxydables présentes dans un échantillon d’eau. Le résultat est donné en mg/l. de DCO. La détermination de la DCO5 peut être réalisée en laboratoire mais aussi à l’aide de flacons de réactifs prêts à l’emploi et d’un incubateur spécial.
– La mesure de la DBO5 ( Demande Biologique en Oxygène) permet de mesurer en laboratoire la quantité d’oxygène consommée par les bactéries dégradant les matières d’un échantillon placé dans l’obscurité à 20° C pendant 5 jours. Le résultat est donné en mg/l. de DBO5. La détermination de la DBO5 s’effectue en général en laboratoire.

Les deux paramètres DBO5 et DCO sont également très utilisés pour comparer la charge polluante des effluents d’entrée et de sortie d’une station d’épuration. Cela permet de calculer le pourcentage de rendement de la station en ce qui concerne l’abattement de la pollution organique..
Au stade d’ammonium (NH4+)
La minéralisation de la fraction « azote » des MO par les bactéries en ammonium, puis nitrites, puis nitrates, s’appelle la nitrification. A ces trois stades, l’azote en excès entraîne des nuisances dans les eaux.
L’AMMONIUM est le principal indicateur chimique de pollution directe, c’est à dire de déséquilibre du milieu.
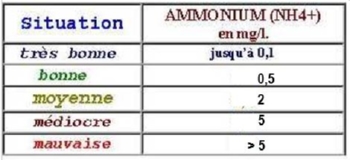
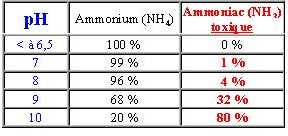
Mais seule une part de l’ammonium peut être toxique pour la faune aquatique (lésions aux branchies des poissons) mais uniquement lorsque l’eau est alcaline. En effet plus le pH (au delà de 6,5) et la température sont élevés, plus une partie importante d’ammonium se transformera en gaz dissous ammoniac (NH3) très toxique dissous dans l’eau.
La toxicité affecte les salmonidés dès 0,02 mg/l. de NH3.
Il existe des tests de terrain pour déterminer la concentration en ammonium de l’eau.
Au stade de nitrites (N02)
L’ammonium est transformé en nitrites par des bactéries nitreuses ( nitrosomas) consommatrices d’oxygène dissous.
Les nitrites sont très dangereux pour les organismes vivants, empêchant l’oxygène de se lier à l’hémoglobine du sang. Une concentration supérieure à 1mg/l est mortelle.
Les nitrites sont des éléments qui peuvent être considérés comme toxiques pour la faune aquatique notamment les poissons. Suivant les conditions et les espèces considérées, des teneurs de 0.01 mg/l à 0.06 mg/l sont, à plus ou moins longue échéance, dommageables.
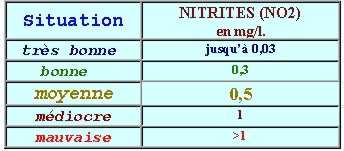
Il existe des tests colorimétriques de terrain (bandelettes) pour déterminer la concentration en nitrites de l’eau.
Au stade des nitrates (N03)
Les nitrites de la rivière sont transformés à leur tour en nitrates par les bactéries nitriques (nitrobacter) consommatrices d’oxygène dissous.
Les nitrates de l’agriculture intensive.
Dans les rivières, les nitrates en excès n’ont pas une origine naturelle. Ils ont pour première source (2/3) l’agriculture intensive. car les cours d’eau sont alimentés par les nappes souterraines, elles même polluées par l’infiltration de « fertilisants » épandus en grande quantité : engrais nitratés des cultures céréalières intensives, lisier des centaines de milliers de cochons des porcheries industrielles.
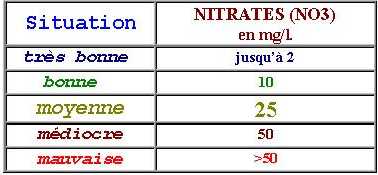
Dans les eaux souterraines, la présence naturelle de nitrates, de l’ordre de 5 à 10mg/l, a été multipliée par l’infiltration des engrais agricoles. C’est dans les régions de plaine, ou à faible relief, que les eaux des nappes souterraines sont le plus envahies par les nitrates ; cette pollution atteint en certains points plus de 50, voir plus de 100 mg/l. de NO3. Cette situation pose aussi problème au niveau des puits destinés à fournir la ressource en eau potable.
( En France, pour être « potable » l’eau du robinet ne doit pas dépasser 50 mg/l. de NO3 et les eaux de surface pompées à cet usage ne doivent pas dépasser cette concentration. Mais, cadeau du législateur à l’agriculture intensive, si l’on puise des eaux souterraines pour la « production d’eau de consommation », il est autorisé de la pomper jusqu’à 100 mg/l. de NO3. Il faudra ensuite, avant de la distribuer, la dénitrifier pour la redescendre à 50mg/l., bien sur aux frais du consommateur….)
Les nitrates résiduaires
La seconde source en importance (1/3), ce sont les rejets résiduaires des agglomérations dont les stations d’épuration transforment la pollution organique en nitrates. (Les stations d’épuration utilisent le cycle de l’azote, artificiellement forcé par suroxygénation des effluents).En cas d’absence ou de déficience de station d’épuration, il y a rejet de matières organiques, d’ammonium ou d’ammoniac, de nitrites…
Les eaux des stations d’épuration peuvent être dénitrifiées par un traitement complémentaire qui transforme l’azote des nitrates en azote atmosphérique.
La surcharge des eaux des rivières en nitrates entraîne leur eutrophisation. Les nitrates associés aux phosphates sont des nutriments présents en excès et qui déclenchent surtout en période estivale une croissance exubérante des algues qui envahissent l’espace aquatique et par la suite « l’asphyxie ». C’est l’ EUTROPHISATION.

L’eutrophisation c’est l’invasion de la rivière par les algues à la « belle saison »…
Au plan de la toxicité pour les êtres vivants, les nitrates n’ont pas la dangerosité des nitrites.
Mais dans le système digestif, la flore bactérienne peut métaboliser les nitrates et produire de la nitrosamine, substance cancérigène pouvant entraîner le développement de cancers gastriques.
Cela a été démontré sur des animaux.
Les nitrates sont aussi accusés de provoquer chez le nourrisson la méthémoglobinémie, affection qui bloque le transport de l’oxygène par l’hémoglobine du sang.
Pour pouvoir continuer allègrement à polluer les nappes et les rivières, le lobby de l’agriculture intensive conteste les problèmes liés à l’utilisation des nitrates agricoles et l’impact sanitaire des nitrates contenus dans l’eau potable.
L’apport de nitrates au corps humain est estimé à 30% pour l’eau et 70% pour l’alimentation.
Mais s’il est vrai que la plus grande part des nitrates absorbée par l’homme provient des légumes issus de l’agriculture intensive (entre 100 et 200 mg de nitrates par jour) et est déjà excessive, il n’est pas sérieux d’en rajouter encore à travers la consommation d’eau.
Il existe des trousses tests colorimétriques de terrain (bandelettes) pour déterminer la concentration en nitrates de l’eau.
